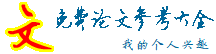| a. Tetraploid,cv. b.Chimeraof diploid and tetraploid c.Diploid,
图3京秀DNA含量分布图
Fig.3 Map of distribution of DNA content of“jingxiu”
2.2.5秋水仙素浓度和浸泡时间对京秀的诱变效果
结果表明,处理当代植株萌发的嫩芽均未测得DNA含量明显加倍的细胞,生根诱导20天后,仍未测得DNA含量明显加倍的细胞,倍性不随生长期的变化而变化。
浸泡茎段诱导京秀葡萄共出现39株变异植株,有17株为四倍体。据表1的数据,短6小时的时间处理和0.05%的低浓度处理均没有出现变异植株中国论文下载中心。当处理时间在6小时以上时,诱变率随着浓度的增加先升高后下降,处理时间越长,最佳处理浓度越低,当高于此浓度时,诱变率开始下降;处理浓度高于0.05%时, 诱变率随着处理时间的增加先升高后下降,处理浓度越高,最佳处理时间越短,当超过此时间时,诱变率开始下降。在本实验中,最佳浓度及时间组合为0.3%浓度处理24小时,四倍体的变异率为10.34%。
2.2.6秋水仙素浓度和时间对京秀的诱变效果
混培法诱导京秀葡萄共出现9株变异植株,有5株为四倍体。从表2中可以得出,短时间处理时各浓度均不能诱导变异,而长时间高浓度处理会使苗成活率受到很大影响。组培苗在培养15天时,各浓度均未出现变异植株;培养30天时,除浓度50mg/L外,各个浓度都测得变异植株,1000mg/L 出现1株四倍体,2000mg/L出现2株四倍体;培养45天时,由于长时间秋水仙素培养对植株根系抑制作用的增强,变异植株只在100mg/L出现1株、500mg/L出现1株,但都为四倍体,且生长正常。在本实验中,30天2000mg/L处理效果最好,该处理诱导出变异植株的嵌合体率为零,四倍体出现率在所有处理中最高为20.00%,占总四倍体植株数的40%。
3.讨论
3.1不同处理方式对多倍体诱导效果的影响
徐德平[5]等人研究发现,利用秋水仙素水溶液浸泡茎段比秋水仙素混合培养基法诱导葡萄多倍体效果更好。在本研究中,浸泡茎段法的四倍体诱导率并不明显高于混合培养基法,但从试验操作和后期生长等情况看,直接浸泡单芽茎段法简单且用药量少,药液更易渗入植物组织,倍性特征在短期内就能显现秋水仙素,有利用早期检测及培养四倍体植株。秋水仙素混入培养基诱导四倍体时,如果选用的组培苗苗龄较大则不易诱变,而如果较小,根比较幼嫩,很容易变黑死亡,从而导致整株植株停止生长甚至死亡。另外,混培法需要逐个位置检验芽变的倍性,以确定哪一部分变异芽可以继代培养,因而混培法的检测成本高,不适合大规模的多倍体诱导。
3.2流式细胞术检测葡萄多倍体的可行性分析
在多倍体鉴定上,过去多采用形态观察和器官组织的间接鉴定或体细胞染色体计数法在显微镜下观察鉴定[3]。间接鉴定法虽然简便,但可靠性低[6],染色体计数法可靠性虽高,但操作复杂,难度较大[7]。利用流式细胞术进行葡萄多倍体检测可以有效避免以上问题,该方法不但省时而且操作简单,准确度和灵敏度极高[8] [9]。流式细胞术在进行果树倍性分析中也有不足之处,国际上还没有一个统一的测量植物核DNA含量的标准参照,使用不同的内标时结果存在误差,使用不同的核荧光染料检测出的结果也有明显的差异[10] [11]。利用流式细胞仪检测植物倍性时,样品碎片过多会干扰DNA的测定 [12],在本实验中,通过选择分生组织,快速切碎,采用多次细胞筛过滤以及延长暗置时间等措施有效地减少了碎片,增加了峰的清晰度,但由于暗置时间延长峰出现了轻微的偏移,所以暗置的最佳时间还有待研究。
参考文献References
[1]ZHAO Yan-hua, WU Guo-liang,YAO Wensheng. Advances on polyploid breeding [J]. Shanxi fruits, 2004,(4): 35-36.
2/2 首页 上一页 1 2 |