论文导读::综合实验试题中加入某物质的作用归纳与解析,教育论文。
论文关键词:综合实验试题中加入某物质的作用归纳与解析
综合试题中经常出现考查新加物质作用的试题,这类试题既能考查学生对物质性质的理解,还能考查学生运用化学反应原理解决实际问题的能力,从而考查学生的化学学科素养。新加入的物质的作用一般从以下几个角度去思考。
一、从发生的反应考虑
从发生的反应来看,新加入的物质作为反应物或生成物,有的使原料溶解;有的提供氧化剂或还原剂;有的是通过反应除去杂质;有的是抑制某些离子水解;有的是抑制某些物质吸收等等。
例1(2011盐城二模):铁氧体可用于隐形飞机上吸收雷达波涂料。一种以废旧锌锰电池为原料制备锰锌铁氧体的主要流程如下:

问题1:酸浸时,二氧化锰被还原的化学方程式为:。
问题2:活性铁粉除汞时,铁粉的作用是(填:氧化剂、还原剂、吸附剂)。
解析:对于问题1,硫酸的作用主要是使锌等固体溶解;根据问题1中的信息“二氧化锰被还原,说明H2O2的作用是还原剂,化学方程式为:MnO2+H2O2+H2SO4=MnSO4+O2↑+2H2O。对于问题2,活性铁粉除汞时,铁粉的作用主要是作为还原剂,使溶液中的汞离子变为汞单质。
例2(2009江苏第15题改编):医用氯化钙可用于生产补钙、抗过敏和消炎等药物。以工业碳酸钙(含有少量Na+、Al3+、Fe3+等杂质)生产医药级二水合氯化钙(CaCl2·2H2O的质量分数为97.0%-100.0%)的主要流程如下:

问题:酸化操作是加入盐酸,调节溶液的pH约为4.0,其目的有:①;②;③。
解析:在酸化操作未加盐酸时,溶液中有过剩的氢氧化钙,所以教育论文,目的之一是除去过剩的Ca(OH)2,使之转化为CaCl2;由于Ca2+在蒸发结晶时(160℃)会部分发生水解,在酸性条件下可以抑制Ca2+水解;另外,在酸性较弱或碱性条件下,氯化钙会吸收空气中的CO2,酸性条件可以抑制CO2的吸收。
二、从反应所需要的条件考虑
若从反应发生的条件考虑,加入某物质的作用,有的是作为催化剂;有的是提供反应所需的温度,如作为燃料燃烧放热提供热量,向溶液中加入硝酸铵可以使溶液温度降低;有的是为了控制溶液的酸碱性以提供反应所需的酸碱性要求,等等。
例1(2008江苏第17题):工业上制备BaCl2的工艺流程图如下:

某研究小组在实验室用重晶石(主要成分BaSO4)对工业过程进行模拟实验。查表得
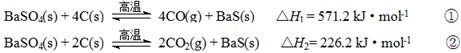
问题:实际生产中必须加入过量的炭,同时还要通入空气,其目的是
,。
解析:加入过量的炭可以使BaSO4得到充分的还原(或提高BaS的产量);由于①②为吸热反应,炭和氧气反应放热可以维持反应所需高温。
例2(2011苏南二模第15题)工业上用粗氧化铜(含杂质FeO)为原料制取氯化铜晶体(CuCl2?2H2O)的生产流程如下:

|
物质
|
Fe(OH)2
|
Cu(OH)2
|
Fe(OH)3
|
|
完全沉淀时的pH
|
≥9.6
|
≥6.4
|
3~4
|
问题:流程中两次加入了CuO,而不是一次性向溶液B中加入过量的CuO,其理由是
。
解析:浓盐酸使CuO、FeO溶解为Cu2+、Fe2+,然后在NaClO作用下,Fe2+转变为Fe3+,加入CuO可控制溶液的PH,使Fe3+变为Fe(OH)3沉淀;Cu(OH)2完全沉淀所需的PH与Fe(OH)3不同,此时通过加入CuO可使Cu(OH)2沉淀出来。所以,CuO应该分两次加入,如果一次性向溶液B中加入过量的CuO,将导致Fe3+和Cu2+同时生成沉淀。
三、从物质的性质考虑
加入某种物质之后可以降低原物质的溶解度,如加入有机溶剂可以降低水的极性,降低一些无机盐在水中的溶解度;可以提高原物质的氧化性,如往高锰酸钾中加入稀硫酸可提高其氧化性;新制氢氧化铜和银氨在碱性条件下可提高其氧化性;有的可以抑制一些离子的水解,如往FeSO4溶液中加入稀硫酸一方面可抑制Fe2+水解;加入某些物质可以防止原物质氧化,常见方法有:①利用一些气体来隔绝空气或氧气,如氢气还原氧化铜结束后,应先停止加热,还要继续通一会儿氢气,让生成的铜在氢气的氛围中冷却;又如在制金属钛时,可以在氩气的氛围中用过量的镁在加热条件下与TiCl4反应制得金属钛;②加入其它更容易被氧化的物质来防止原物质被氧化;③通过加入某物质可以把原物质中的某些官能团保护起来,防止在后面的反应中被氧化,等等。
例1(2010江苏第18题):正极材料为LiCoO2的锂离子电池被广泛用作便携式电源。但钴的资源匮乏限制了其进一步发展。(1)橄榄石型LiFePO4是一种潜在的锂离子电池正极材料教育论文,它可以通过(NH4)2Fe(SO4)2、H3PO4与LiOH溶液发生共沉淀反应,所得沉淀经80℃真空干燥、高温成型而制得。问题:共沉淀反应投料时,不将(NH4)2Fe(SO4)2和LiOH溶液直接混合的原因是。
解析:此题有一定的难度,能很好地考查学生的分析问题能力。此题很容易答成OH-会与NH4+反应。从目标产物LiFePO4来看,即使OH-与NH4+反应对产物没什么影响,关键分析为什么要加入H3PO4而不是把两者直接混合,加与不加H3PO4的区别在什么地方,这样容易得出未加磷酸溶液显碱性,加入磷酸碱性降低,可能酸碱性对Fe2+的还原性有影响,这样经过分析可得出答案:Fe2+ 在碱性条件下更易被氧化论文网站大全。
例2(2011南京二模)PCl3可用于半导体生产的外延、扩散工序。有关物质的部分性质如下:
 问题:右图是实验室制备PCl3的装置(部分仪器已省略)。向甲中通入干燥的Cl2之前,需先通入一段时间 问题:右图是实验室制备PCl3的装置(部分仪器已省略)。向甲中通入干燥的Cl2之前,需先通入一段时间
CO2,目的是 。
解析:由于PCl3遇O2会生成POCl3,遇水生成H3PO3和HCl,通入一段时间的CO2可以排尽装置中的空气,防止生成的PCl3与空气中的O2和水反应。
例3:绿矾(FeSO4·7H2O)是治疗缺铁性贫血的特效药。下面是以商品级纯度铁屑(含少量锡等杂质)生产绿矾的一种方法:

已知:在H2S饱和溶液中,SnS沉淀完全时溶液的pH为1.6;FeS开始沉淀时溶液的pH为3.0,沉淀完全时的pH为5.5。
问题:操作II在溶液中用硫酸酸化至pH=2的目的是;通入硫化氢至饱和的目的是:
①除去操作I所得溶液中含有的Sn2+等杂质离子;②。
解析:控制溶液的PH可以抑制一些离子的水解。根据题给信息,SnS沉淀完全时溶液的pH为1.6,而FeS开始沉淀时溶液的pH为3.0,所以,操作II在溶液中用硫酸酸化至pH=2的目的是使Sn2+完全变成SnS沉淀,而Fe2+不沉淀。由于硫化氢本身是一种强还原剂,所以,通入硫化氢至饱和的目的是除了除去操作I所得溶液中含有的Sn2+等杂质离子之外,还可以防止Fe2+被氧化。
四、从反应速率考虑
通过加入某物质以加快反应速率。常见的方法有:通压缩空气(相当于搅拌)、鼓热空气或热水蒸气(相当于加热和搅拌);加入催化剂;加入的物质与原来物质构成原电池(如实验室用锌粒与稀硫酸反应制氢气,为了加快反应速率可以加少量铜粉或硫酸铜溶液),等等。
例题(2011南京二模) “废铁屑为原料生产莫尔盐的主要流程如下:

问题:“反应I”中通入N2的作用是。
解析:加入N2一方面可以防止空气中的氧气进入防止Fe2+被氧化为Fe3+,而且起搅拌作用,以加快反应速率。
又如工业上从海水中提取溴时,先往已提取氯化钠的苦卤中通入氯气,得到溴水,然后鼓入热空气,此处热空气的作用有两点:其一由于是“热”空气,能降低溴在水中的溶解度,因为气体溶解度随温度升高而下降;其二,溴能以溴蒸气的形式随空气一起出来。
五、从化学平衡考虑
1.从转化率考虑
例如教育论文,用乙酸和乙醇制乙酸乙酯时为了提高乙酸的转化率可采用:再加入乙醇;加入浓硫酸吸水;及时蒸出乙酸乙酯,等等。
例题:我国自行研制的优质磷酸二氢钾(KDP)晶体被应用于大功率固体激光器中。现以氯化钾和磷酸为原料制取磷酸二氢钾,反应方程式为:
以下是在三正丁胺中制备磷酸二氢钾的工艺流程:

已知:三正丁胺是不溶于水的有机溶剂,与氯化氢反应生成一种可溶于水的盐,能使磷酸二氢钾在水中的溶解度降低
问题:使用三正丁胺能促进该反应进行的原因是 。除该方案外,促进该反应进行还可采取的措施有。
解析:根据已知信息,三正丁胺能降低KH2PO4的溶解度,使其析出后,降低了生成物浓度;同时生成的HCl与三正丁胺反应,也降低了HCl的浓度,使平衡向正反应方向移动。
2.从沉淀的转化考虑
实现沉淀转化一般可以通过以下方法:加入试剂生成更难溶的物质;增大离子浓度使Qc>Ksp,从而产生沉淀。
例如(2011南通二模):高铁酸钾(K2FeO4)是一种新型、高效、多功能水处理剂,且不会造成二次污染。已知高铁酸盐热稳定性差,工业上用湿法制备高铁酸钾的基本流程如下图所示:

问题:结晶过程中加入浓KOH溶液的作用是: 。
解析:Fe(OH)3与KClO在碱性条件下会产生K2FeO4,加入浓KOH溶液,C(K+)会增大,有利于生成K2FeO4沉淀。
六、从产品的组成考虑
有时化工生产中经过一系列操作之后,产品的元素组成比不符合要求,可以再加入一些物质以调节元素的组成比。例如第一部分中的例题1,可以设计这样的问题:同时加入MnSO4和铁粉的目的是。
参考答案:可以调节滤液离子的成分,符合水热后获得锰锌铁氧化体的组成(二次加入铁粉还可进一步除去汞)。
|