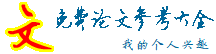图.3 光照和呼吸抑制剂光合速率的影响。星号代表与对照间存在显著性差异(P < 0.05)
Fig. 3. The effects of illumination and respiration inhibitors on photosynthetic rate of poplar
leaves. The asterisk indicates astatistically significant difference from control (P < 0.05).
我们也利用叶绿素荧光仪调查了呼吸抑制剂对叶片叶绿素荧光参数的影响。结果发现,在4小时光照过程中,呼吸抑制剂并没有对光照下光系统II电子传递的最大量子效率(Fv'/ Fm')造成影响。在前3小时光照过程中,呼吸抑制剂也并没有对光照下光系统II的实际光合效率(ФPSII,(Fm'-Fs)/Fm')和光化学荧光淬灭系数(qP)造成影响;但在4小时光照后,SHAM和KCN的单独处理均导致了ФPSII和qP显著性的降低,而SHAM和KCN的复合处理对ФPSII和qP的抑制作用较之SHAM和KCN的单独处理更为明显(图.4)。



图.4 光照和呼吸抑制剂对叶绿素荧光参数的影响。星号代表与对照间存在显著性差异(P < 0.05)龙源期刊。
Fig. 4. The effects of illumination and respirationinhibitors on chlorophyll a fluorescence quenching parameters of poplarleaves. The asterisk indicatesa statistically significant difference from control (P < 0.05).
3 讨论
我们的研究发现,持续的光照在增加杨树叶片异戊二烯释放的同时,也增加了其总呼吸、细胞色素途径和交替呼吸途径的容量,暗示了呼吸作用在光诱导的异戊二烯的释放过程中可能扮演着积极的角色 (图1、2)。为了明确这一问题,我们在光照前用SHAM (交替呼吸途径抑制剂)和KCN (细胞色素途径抑制剂) 预处理了杨树叶片。结果显示,在前3小时光照下,呼吸抑制剂的处理并没有对叶片异戊二烯的释放造成显著性的影响;而在4小时光照后,尽管SHAM和KCN的单独处理仍然没有显著性地影响异戊二烯的释放水平,但SHAM和KCN的复合处理显著性地降低了叶片异戊二烯的释放。这显示了呼吸的抑制会降低异戊二烯的水平,表明呼吸作用有利于光诱导的异戊二烯的释放。
如前文所述,异戊二烯的释放依赖于光合作用[3]。基于此,我们调查了是否呼吸抑制剂是通过影响光合而改变了异戊二烯的释放。结果显示,在4小时光照过程中,叶片的光合速率有着一定程度的上升。呼吸抑制剂对光合的影响与其对异戊二烯释放的影响相似,表现为前3小时光照下呼吸抑制剂没有显著性地影响光合速率;而在4小时光照后,两种抑制剂的复合处理显著性地降低了光合速率(图4)。
目前的研究发现生物论文,在光合作用的运行过程中,叶绿体和线粒体之间存在着密切的联系。在光合组织中,叶绿体将光能转化为能量和还原力以用于二氧化碳的固定,但是光合作用只能使用所吸收光能的50%用于固定二氧化碳,这就不可避免地导致了在叶绿体中过多还原力的积累。如果这些过多的还原力没有被消散就会导致叶绿体中活性氧的不断积累,从而对光合作用中重要蛋白造成氧化损伤并降低光合作用[12]。而植物可以通过苹果酸-草酰乙酸穿梭等系统将叶绿体中过多的还原力传递到线粒体,并被线粒体的呼吸电子传递所消散。因此,线粒体的电子传递系统在优化光合作用中扮演着重要的作用[4, 5, 13] 。利用叶绿素荧光仪检测发现,在4小时光照过程中,呼吸抑制剂并没有对光系统II的光合效率造成影响。但在4小时光照后,SHAM和KCN的单独处理均导致了光系统II实际光合效率(ФPSII)显著性降低,而两种抑制剂的复合处理对ФPSII的抑制作用较之单独处理更为明显。由于这种显著的抑制作用在前3小时的光照过程中并没有出现,这可能表明了当光能积累到一定程度时,呼吸作用对维持光合电子传递能力起到了一定的作用。我们也注意到,在抑制剂处理的叶片中ФPSII的降低总是密切联系着光化学荧光淬灭系数(qP)的降低。因为qP值的大小反映了光系统II的氧化水平,qP的降低表明了当光能积累到一定程度时呼吸作用能够在一定程度上避免光系统II的过分还原。
综上,这些结果表明了呼吸作用可能通过优化光合作用的正常运行而有助于光照下植物异戊二烯的释放,这种作用在光能持续积累过程中变得更加明显。
参考文献
1.GuentherA B, Hewitt C N, Erickson D, et al. A global model of natural volatile organiccompound emissions [J]. Journal of Geophysical Research, 1995, 100(D5): 8873–8892.
2.Sharkey T D, Wiberley A E, Donohue A R.Isoprene emission from plants: why and how [J]. Annals of Botany, 2008, 101: 5–18.
3.Sanadze G A. Biogenic isoprene(a review) [J]. Russian Journal of Plant Physiology, 2004,51: 729–741.
4.Ribas-CarboM, Robinson S A, Gonzalez-Meier M A. Effects of light on respiration and oxygenisotope fractionation in soybean cotyledons [J]. Plant, Cell and Environment, 2000, 23:983–989.
5.Padmasree K, Padmavathi L,Raghavendra A S. Essentiality of mitochondrial oxidative metabolism forphotosynthesis: optimization of carbon assimilation and protection againstphotoinhibition [J]. CriticalReviews in Biochemistry and Molecular Biology, 2002, 37: 71–119.
6.FengH, LiH, LiX, et al. The flexible interrelation between AOX respiratorypathway and photosynthesis in rice leaves. PlantPhysiology and Biochemistry, 2007, 45: 228–235.
7.Bartoli C G, Gómez F, Gergoff G, et al. Up-regulation of the mitochondrialalternative oxidase pathway enhances photosynthetic electron transport underdrought conditions [J]. Journalof Experimental Botany, 2005, 56: 1269–1276.
8.VanlerbergheG C, McIntosh L. Alternative oxidase: from gene to function [J]. AnnualReview of Plant Physiology and Plant Molecular Biology, 48: 703–734.
9.Yoshida K, Terashima I, Noguchi K. Distinctroles of the cytochrome pathway and alternative oxidase in leaf photosynthesis [J]. Plant and Cell Physiology, 2006, 47(1): 22–31.
10.Zeidler J, Lichtenthaler H K. Twosimple methods for measuring isoprene emission of leaves
byUV-spectroscopyandGC-MS[J].Z.Naturforsch,1998,53c:1087–1089.
2/2 首页 上一页 1 2 |